Doria cobra 'senso de urgência' da Anvisa para aprovar Coronavac

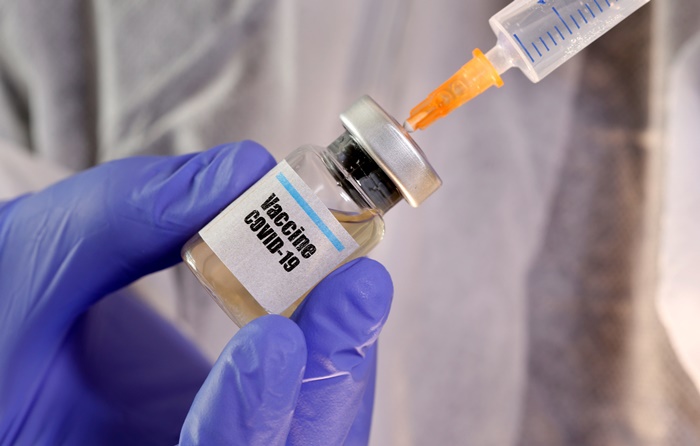
Um dia depois de a Agência Nacional de Vigilância Sanitária (Anvisa) afirmar que faltam documentos para avaliar o pedido de uso emergencial da Coronavac, vacina contra a covid-19 desenvolvida pelo Instituto Butantã em parceria com a farmacêutica chinesa Sinovac, o governo de São Paulo João Doria (PSDB) cobrou "senso de urgência" do órgão.
"Ritos da ciência devem ser respeitados, mas devemos lembrar que o Brasil perde cerca de mil vidas por dia para a covid-19", tuitou. "Com a liberação da Anvisa, milhões de vacinas que já estão prontas poderão salvar vidas"...






.jpg)



.jpg)
.jpg)

.jpg)
.jpg)


.jpg)
.jpeg)

.jpg)

.jpg)










