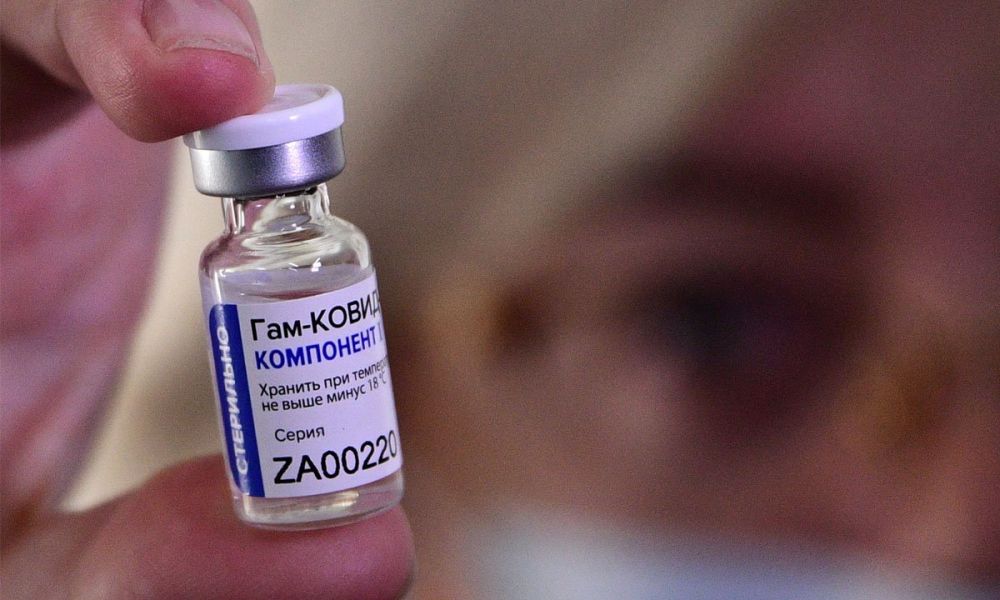
O governador da Bahia, Rui Costa, disse na manhã desta sexta-feira (30) que espera mais proatividade da Agência Brasileira de Vigilância Sanitária (Anvisa) com relação à análise da vacina russa Sputnik V. Rui sugeriu que a agência brasileira realizasse testes ou buscasse informações técnicas nos mais de 60 países que já aprovaram a aplicação do imunizante em sua população, a exemplo da Argentina e do México. O governador disse que, caso fosse autorizado, vacinaria a população baiana com a Sputnik, incluindo ele mesmo e sua família.
"Não conseguimos entender, lá no ano passado, início da pandemia, quais foram os padrões científicos que a Anvisa usou para entrar na Justiça para impedir estados e municípios de monitorar quem possivelmente estivesse contaminado, nos aeroportos, medindo a temperatura e oferecendo teste de Covid. Me pareceu à época um parâmetro muito mais de defesa da corporação que um padrão técnico", disse Rui Costa, ressaltando que, da mesma forma, não entende a postura da Anvisa com relação à vacina Sputnik V, já aplicada em mais de 20 milhões de pessoas em todo o mundo...
.jpg)









.jpg)
.jpg)

.jpg)
.jpg)

.jpg)
.jpg)

.jpg)